第584号 2007(H19).03発行
PDF版はこちら
農業と科学 平成19年3月
本号の内容
§微量元素よもやま話[4]
フッ素
京都大学名誉教授
高橋 英一
§育苗箱全量施肥・密植栽培による高品質・良食味米の安定生産
秋田県農林水産技術センター農業試験場
主任研究員 金 和裕
微量元素よもやま話[4]
フッ素
京都大学名誉教授
高橋 英一
フッ素の発見1)
フッ素(F)はハロゲン族四兄弟(フッ素,塩素,臭素,ヨウ素)の長兄にあたりますが,発見されたのは一番あとです。しかし天然のフッ素化合物である螢石(CaF2)は古くから鉱石の溶融剤として利用されていました。
1771年スウェーデンのシェーレ(Scheele)は,螢石の粉末を硫酸と熱したところ,ガラスのレトルトの内面が腐食されて不透明になるとともに*1,主として石膏(CaSO4)からなる白い物質がレトルトの底に沈澱し,螢石のカルシウムに結合していた酸性物質が受器へ追い出されることに気づきました。シェーレはこの実験から,螢石は未知の酸で飽和された石灰土から成ると考えました。そして発生した酸に石灰水を加えると,天然の螢石に似た人工の螢石が得られました。この一連のプロセスはつぎのようであったと思われます。
CaF2+H2SO4=2HF+CaSO4
6HF+SiO2=H2SiF6+2H2O
2HF+Ca(OH)2=CaF2+2H2O
シェーレの得た酸は当時「スウェーデンの酸」と呼ばれていましたが,それはケイフッ酸(ガラスのシリカにフッ化水素が反応して生じたH2SiF6)の混じった不純なフッ化水素酸(HF)でした。それから40年近くたった1809年,フランスのゲイ・リュサック(Gay-Lussac)とテナール(Thenard)は鉛のレトルトの中で螢石を硫酸と熱して,比較的純粋なフッ化水素酸を得ましたが,二人とも実験中にひどい中毒にかかりました。
その後このフッ化水素酸からフッ素を単離しようと,何人もの化学者が試みましたが成功しませんでした。それは実験装置の材質と直ちに反応するフッ素の激しさを抑えることができなかったためでした。しかし1886年になってフランスのモアッサン(Moissan)は,銅製のU字形の容器を用いることによってフッ素の単離に成功しました。銅を用いると容器の表面にフッ化銅(CUF2)ができて保護されるからです。
彼は無水のフッ化水素(液体)に,電導性を与えるためにフッ化水素カリウム(KHF2)を溶かし,白金-イリジウム合金の電極を用いて電気分解を行いました。すると陰極に水素,陽極にフッ素が発生し,フッ素を銅の管の中に集めることに成功しました。
この新元素の名前Fluorine(フッ素)は,それを単離するのに用いた鉱石fluorite(螢石)に因んで付けられました。fluoriteのfluorはラテン語のfluere(流れる)に由来しますが,鉱物を精錬する場合螢石を混和して熱すると容易に溶けて流動しやすくなることから,この名前が与えられていました。元素名は原鉱石の名をとっただけで,「流れる」という原意とは関係はありません。
フッ素は単離されたものの貯えるのが容易ではないので,工業的に利用されるようになるのは,発見から50年以上もたってからでした。そのきっかけは,原子爆弾製造のために大量のフッ素が必要になったからでした。
原子爆弾には中性子で核分裂を起こしやすいウランの同位元素235Uが必要ですが,天然のウランには235Uは0.7パーセントしか含まれておらず,残りの99.3パーセントは分裂を起こしにくい238Uです。235Uと238Uは化学的性質が同じであるため,235Uを分離濃縮するには両者の僅かな重さの違いを利用するしかありませんでした。
そこでとられたのが「気体拡散法」と呼ばれる方法で,ウランをフッ素と化合させてガス状の六フッ化ウラン(UF6)にし,薄い多孔壁を通過させます。その際軽い235Uは238Uより速く隔壁を通り抜けるので,それを何千回と繰り返すと235Uだけの六フッ化ウランを取り出すことが出来ます*2。これを原料として原子爆弾に必要な金属ウラン235Uを得たのでした。
これには大量のフッ素が必要であるため,この元素の扱い方が研究された結果,大量利用が可能になり,それは後にテフロンやフレオンなどの有用なフッ素化合物*3を生産するフッ素工業が発展するもとになりました。
環境中のフッ素2)
フッ素のクラーク数は0.03パーセントで塩素の6分の1ですが,岩石圏あるいはその風化層である土壌では塩素より高くなっています(表1)。塩素のクラーク数が高いのは,水圏(海水)中の塩素によっています。そしてそれは原始大気中の塩化水素ガスに由来しています*4。
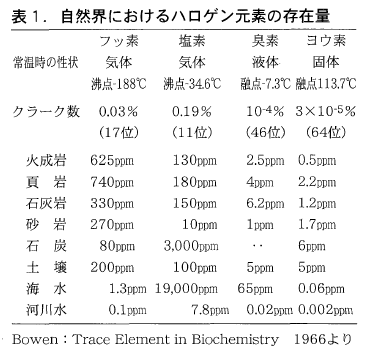
フッ素は親石性の強い元素といわれ,地殻中のケイ酸塩鉱物に多く含まれています。フッ素(F⁻)のイオン半径は1.33Aで水酸基(OH⁻)のイオン半径と等しいため,水酸基を含むケイ酸塩鉱物に同形置換で入りやすいからです。したがってシリカ含量の高い岩石や土に多い傾向がみられます。
フッ素はハロゲンイオンの中で特殊な行動を土壌ー植物生態系で示すことが,結田氏らによって報告されています3)。すなわち土壌による吸収率はF⁻のみが高く,添加F⁻(0.1-1000ppmの範囲)の75~99%が吸収されたが,Cl⁻,Br⁻,I⁻は殆ど吸収されませんでした。さらにイネ幼殖物による吸収は,水溶液からの場合はBr⁻>Cl⁻>>F⁻>I⁻の順で,F⁻はI⁻とともに吸収されにくいグループに属するが,土壌からの場合はBr⁻>Cl⁻>>I⁻>>F⁻の順で著しく低く,F⁻の土壌による吸収が他の三つのハロゲンイオンにくらべて特異的に高いことを反映していました。
また土壌中の塩素が動きやすく,土壌水の動きによって土壌から溶脱したり集積したりするのに対して,フッ素が動きにくいことは,土壌と河川水のフッ素濃度を比べると分かります(河川水/土壌濃度比はF0.0005,Cl0.08でFはClの160分の1になっている)。
フッ素を含む鉱物としては螢石(CaF2),氷晶石(Na3AlF6),燐灰石(フルオロアパタイトCa10P6O24F2)などがあります。これらの鉱物を多く含む土壌には1000ppm以上のフッ素を含むものがあり,そのような土の付着した草を食べる家畜がフッ素中毒に罹ることがあるそうです。
河川水,地下水(井戸水)中のフッ素は,飲料水を介して歯の疾患に関わることがあるので,各国で調査が行われています。フッ素濃度は地域による変動がかなりありますが,わが国の43河川の平均値として0.15ppmという報告があります。また福岡県下の飲料水として用いられている地下水,井戸水,水道水でそれぞれ平均0.30,0.31,0.32ppmの値が得られています。これら通常の陸水に比べると海水のフッ素濃度は1.3ppmと,かなり高くなっています。
大気中のフッ素の給源は,火山ガス以外はタイルやリン酸肥料やアルミニウムなどの製造工業から発生する人為的原因によるものです。これらは原料の石炭,粘土,リン鉱石や,アルミニウム製造の際融剤として用いられる螢石などに含まれていたフッ素が,熱や酸処理によって揮散したものです。
たとえばリン鉱石は3~4パーセントのフッ素を含んでいますが,過リン酸石灰製造中にその1/2~1/3が,フッ化水素(HF)やリン鉱石中のSiO2に作用して生じた四フッ化ケイ素(SiF4)の形で揮散します。これらの工場周辺で局地的に発生するガス状のフッ化物は,植物の光合成を阻害するなどして,農作物に被害をもたらすことがあります。
動物とフッ素
フッ素は動物にどのくらい含まれているのでしょうか。動物の体は大きく分けて軟組織と硬組織があります。軟組織は生命現象を発現する代謝の営まれている場であり,硬組織は体を物理的に保護したり支えたりする殻や骨の部分です。軟組織のフッ素含量は数~数十ppm程度であるのに対し,硬組織のそれは数百ppmという高さで,フッ素は動物の硬組織に著しく多い(集積する)という特徴があります。
表2に動物の硬組織のフッ素含量の分析値を示しましたが,脊椎動物の骨や歯,無脊椎動物(棘皮,節足,軟体,腔腸動物)の殻のフッ素含量の高いことが分かります。これは骨や殻の主成分であるリン酸カルシウムや炭酸カルシウムに,フッ素が捕捉されるためです。また海産の魚類や無脊椎動物に多い傾向ありますが,これは陸水に比べて高い,海水のフッ素濃度の影響と見られます。

動物におけるフッ素の役割としては硬組織の強化があげられます。飲料水のフッ素濃度と虫歯の発生率との間に逆相関が見られるという調査結果から,歯の表面の琺瑯質中のフッ素に虫歯予防効果が期待されるとして,水道水のフッ素処理が試みられたことがあり,また歯磨剤へのフッ化物の添加も行われています。
脊椎動物における骨化は,先ずカルシウムとリン酸が沈着するマトリックスをコラーゲン蛋白がつくり,ついで鉱物質のヒドロキシアパタイトCa10(PO4)6(OH)2が形成されますが,F⁻はOH⁻と互換性があるのでヒドロキシアパタイトとフルオロアパタイトが共存します。歯のアパタイト結晶中にとりこまれたフッ素は結晶を安定化するため,口内細菌によってつくられる乳酸,酢酸などによる脱灰に対する抵抗性を高め,虫歯の予防に貢献すると考えられます。
一方一種の風土病である斑状歯(歯に縞模様の白濁を生じ,進行すると着色し,重いと歯の先端が崩れる)は,飲料水中のフッ素過多が原因といわれています。これはフッ素が歯質形成期の細胞の機能を阻害し,エナメル質の石灰化不全を引き起こすためと考えられています。
フッ素の摂取が有益な場合と有害になる場合との幅(濃度差)は狭いので,飲料水中のフッ素濃度の適量値(eufluorosis level)が各国で定められています。因みにわが国の水道法では,フッ素の最大許容濃度は0.8ppmになっています。
植物とフッ素
フッ素は土の中には数十~数百ppmの範囲で存在していますが,一般の植物のフッ素含量は乾物当たり10~20ppm程度で40ppmを超えることはまれです。ところが茶樹の成熟葉では500~1000ppmも含まれ,数千ppmに達する場合もあります。火山灰土にはかなりのフッ素が含まれており,鹿児島の桜島付近に生育する茶樹の葉で,8,200ppmものフッ素含量が報告されています2)。
茶樹は酸性土壌に強く,アルミニウム含量が高いという栄養特性がありますが,茶樹におけるフッ素とアルミニウムの関係について,京都府立大学の山田秀和氏の興味深い研究があるので紹介します4,5)。
土の中の可溶性フッ素は総量の10分の1以下で,遊離のフッ素イオン(F⁻)は殆どなく,土のpHが5以上ではリン酸カルシウムと結合してフッ素アパタイト(3Ca3(PO4)2・CaF2)として,またpHが5以下の酸性土壌ではアルミニウムと結合してフッ化アルミニウム錯イオン(AIF2⁺,AIF⁺⁺) として存在しています。したがって,酸性の強い茶園土壌から茶樹が吸収するフッ素の形態は,フッ化アルミニウムであると思われます。
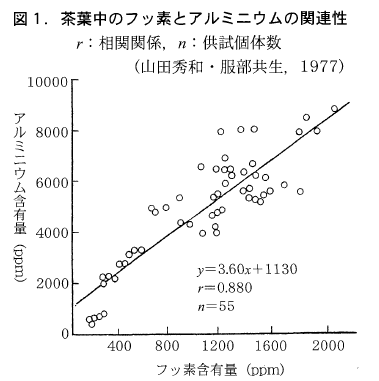
これを裏書きするように,茶葉中のフッ素とアルミニウムの間には高い相関がみられます(図1)。茶葉中のフッ素・アルミニウム比(F/Al)は同一茶樹では葉位に関わらずほぼ一定で,この値は品種に関係なく生育土壌に依存しています。これは土壌溶液中のAl⁺⁺⁺,AIF⁺⁺,AIF2⁺の分布を支配するフッ素イオン濃度が異なるため,茶園ごとに茶葉のF/Al比に差異が生じるものと思われます。
茶樹のほかに同じツバキ科のサザンカ,ツバキ,ヒサカキ,ハマヒサカキにもフッ素とアルミニウムの集積が認められます。しかしナツツバキ,ヒメシャラ,サカキではアルミニウムの集積は認められるもののフッ素含量は数十ppmと少なく,さらにモッコクでは両方とも少なくなっています(表3)。
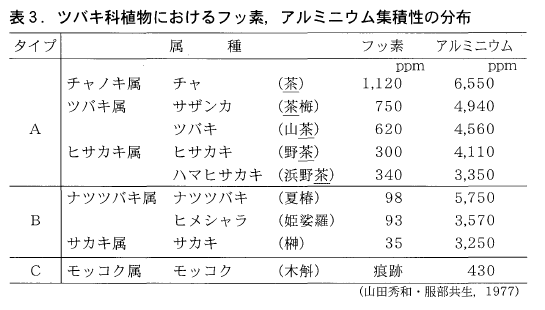
つまりツバキ科の植物には,フッ素とアルミニウムに関してA,B,Cの三つのタイプが存在しています。タイプAの植物は茶樹と同様にAl⁺⁺⁺,AIF⁺⁺,AIF2⁺の形でアルミニウムとフッ素を吸収するのに対して,タイプBの植物はAl⁺⁺⁺の方を吸収し,タイプCはAl⁺⁺⁺もあまり吸収しないのではないかと思われます。またフッ素集積性の植物名には何故かみな「茶」の字が使われています(お茶の代用にされていたためでしょうか)。これらの結果は,植物のフッ素吸収にはアルミニウムが必要だが,アルミニウムの吸収にはフッ素は必ずしも必要でないことを示唆しています。
このように茶葉にはかなりのフッ素が含まれていますが,われわれが飲む「お茶」の中にはどれくらい溶けてくるのでしょうか。表4はその一例ですが,発酵ないし半発酵させた茶(紅茶,ウーロン茶)は,非発酵の緑茶より溶出率が高い傾向がみられます。一般の食品のフッ素含量は低いので,茶は有望なフッ素の供給源です。因みに一日に10グラムの番茶(400ppmのフッ素を含む場合)を用い,その10パーセントが溶出されたとすると,0.4mgの摂取量になりますが,これは所要量(1.5mg/日)の4分の1に相当します。

また茶の葉を食う茶毒蛾の体には高濃度のフッ素が集積していますが(表5),このフッ素は茶毒蛾にどのような影響を及ぼしているのでしょうか。茶樹はフッ素を集積することによって何か利益を得ているのではないかと思われますが,現在のところ明らかになっていないようです。

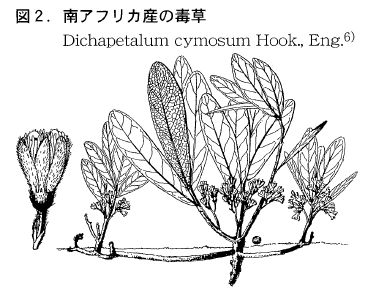
南アフリカ産のトウダイグサ科のDichapetalum cymosum(図2)は,乾物当たり200ppmものフッ化物を含んでいますがその葉は毒性が強く,ヒツジを殺すのに25グラムで十分といわれています。その原因は乾物当たり50ppmを占めているフルオロ酢酸(CH2FCOOH)です。これは摂取した動物の体内でフルオロクエン酸に変換し,クレブス回路の酵素アコニターゼを桔抗阻害します。しかしこの反応はDichapetalum cymosumでは起こらないため,害作用をまぬがれていると思われます6)。
微量元素としてのフッ素の位置づけ
1930年代に風土病の斑状歯が飲料水中のフッ素によることが明らかにされ,ついで斑状歯の多い地域は虫歯が少ないことが発見されフッ素に対する関心が高まりました。また高フッ素地域では低フッ素地域にくらべて,骨硬化症(osteosclerosis)が発症する一方で,骨粗しよう症(osteoporosis)は少ない傾向のあることも認められています。これらの疫学的知見は,脊椎動物の骨化にフッ素の過剰・不足が影響を及ぼすことを示しています。
そこでフッ素が必須元素であるか否かを明らかにするために,動物実験が行われました。すなわちラットに高度に精製したフッ素含量の非常に低い食事を与えたグループと,同じ食事に少量のフッ素を添加したグループとの比較が,多くの研究者によって行われました。しかし結局両グループとも,生長も繁殖も,歯や骨の構造にも異常は認められませんでした7)。
このような動物実験と疫学的研究との間のギャップは,一考に値すると思います。疫学というのは人間の集団を対象にして,伝染病の原因や動向を究明する医学の一分野として始まりましたが,その後広く健康を損ねる原因を研究対象にするようになりました。斑状歯,虫歯,骨硬化症,骨粗しょう症もその例ですが,これらの病症の原因は単一なものではなく,年齢,性差,体質,生活習慣などいろいろな要因が関係します。しかし特定の人間集団を対象にするときは,それらの要因の一つが原因として浮かび上がってくることがあります。フッ素はそのような例でしょう。
しかしフッ素が生存のために摂取する必要があること,すなわち必須元素であることを証明するにはフッ素の欠如実験が必要になります。ラットを使った動物実験は,フッ素が必須元素であることを示す結果は得られませんでしたが,フッ素の完全な除去(骨中にフッ素を含まないラットを育てること)に成功していないので,問題が残ります。つまり虫歯や骨粗しよう症予防にフッ素の効果がみられる条件を明らかにする課題が残っています。
このフッ素をめぐる状況は,作物に対する栄養元素としてのケイ素の位置づけについての研究を思い起こさせます。自然条件下では,イネを初めとするケイ素集積性の作物が健全な生育をするのに,ケイ素が必要であることが知られています。そこでケイ素の必須性を検証するためにケイ酸欠如栽培が行われましたが,生物的非生物的ストレスの無い条件にしてやれば,植物としては正常に生育します。
この場合もケイ素を全く含まない作物は得られていないので問題は残りますが,ケイ素の効果が現れる条件が究明され,またその理由も明らかにされたので,ケイ素は有用元素あるいは農学的必須元素の地位を与えられています。自然の中の植物はいろいろなストレスにさらされていますが,ケイ素は環境ストレスに対する耐性を高める働きをすることが分かったからです。
植物でもフッ素の必須性は明らかにされていません。しかし中には茶樹やツバキなどのようにフッ素を集積する植物があります。このような特性が保存されているのは,自然界での種の保存に有利なことがあるからではないでしょうか。ケイ素の場合のようにフッ素集積という栄養特性の意義が明らかにされてほしいと思います。
生物は長い進化の過程でいろいろな元素を試してきました。われわれはそれらの中のいくつかの元素を,多量必須元素,微量必須元素,有用元素あるいは単なる有害元素として認識していますが,手つかずの未知の元素はまだまだ沢山残っており,興味は尽きません。
*1 1670年ニュルンベルグのガラス切り職人であったシュヴァンハルト(Heinrich Schwanhard)は,螢石を強い酸で処理すると眼鏡のレンズが腐食されることに気付いた。彼はこの発見にヒントを得て,ダイヤモンドなどの研磨剤を用いないで,ガラスの表面に模様を描く方法を考案した。即ちガラスをワニスで覆い,それを削って図柄を描き,
彼の腐食液(フッ化水素酸)で処理した後ワニスを取り除くと図柄が現れる1)。
⁺2 235Uを分離濃縮するための巨大な気体拡散工場が,テネシー州オークリッジに建設された(1942年9月起工,1944年完成,原子爆弾に使えるくらいの濃縮度をもった量のウランを生産できるようになったのは1945年の春)。この分離工場はウラン気体を処理する約48万kmに及ぶステンレス・スチールのパイプをもっている。このパイプの長さを伸ばしてゆくと,地球から月に到達してもなお余りがある。ウラン気体が一つの篩い,つまり多孔質の壁を通って拡散あるいは濾過されるたびに,反対側で235Uの含有量がごくわずか増える。このわずかに濃縮された気体を数千回も繰り返し拡散していくと,約95%の238Uと5%の235Uになるまで235Uを濃縮することができた。この工場の総工費は5億5000万ドルにのぼり,更にウランガスを送るポンプを運転するのに大量の電力が必要なため,新たに火力発電所も建設された。[R.E.ラップ著,八木勇訳:発見への道118頁 岩波書店(1961)]
*3 テフロン(Teflon)はフッ素樹脂の商品名で,CF2=CF2の重合体。不燃性,有機溶媒に不溶,化学薬品に対して非常に安定,熱にも安定で電気の絶縁体としてもすぐれているなど多くの長所をもち,いろいろな工業製品に利用されている。
フレオン(Freon)はdu Pont社が最初に製造したフルオロカーボンの商品名。フルオロカーボンはフッ素を含む炭素化合物の総称でCCl3F(F-11),CCl2F2(F-12),CClF3(F-13)などがある。不燃性で毒性や腐食性がなく,化学的にも安定なため噴霧剤や冷媒などに多くの用途をもっている。
*4 創成期の火の玉地球が次第に冷え,表面の温度が300℃台まで下がったとき,地球を厚く取りまく原始大気中にあった大量の水蒸気は水に変わった。そして塩化水素ガスを溶かし込んで雨となって地表に降り注ぎ,強酸性の海をつくった。この原始の海は地球表層の岩石に作用し,その中の塩基成分を溶かしだして中和され,最終的に現在の塩化ナトリウムを主成分にする海水になった。
参考文献
1)ウィークス,レスター著,大沼正則監訳:
元素発見の歴史3-フッ素 朝倉書店(1998)
2)松浦新之助,国分信英著:
フッ素の研究東京大学出版会(1973)
3)結田康一・渋谷政夫・野崎正:
ハロゲン元素(特にフッ素)の土壌による吸収,溶脱および水稲幼植物による吸収 日土肥誌,46(1)9(1975)
4)山田秀和:茶樹とフッ素-アルミニウムとの関連性 化学と生物,15,362-364(1977)
5)山田秀和:ツバキ科植物のフッ素吸収に関する生物地球化学的研究 京都府立大学学術報告・農学 第32号138-170(1980)
6)E. J.ヒュイット,T.A.スミス共著,鈴木米三,高橋英一共訳:
植物の無機栄養,213頁,理工学社(1979)
7)日本化学会訳編:E. J. Underwood微量元素-栄養と毒性-,369-370頁,丸善(1975)
育苗箱全量施肥・密植栽培による
高品質・良食味米の安定生産
秋田県農林水産技術センター農業試験場
主任研究員 金 和裕
1)はじめに
これまで,水稲の栽培技術は時代のニーズにより収量・品質・食味の向上を主目的として改善が進められてきた。しかし,近年の地球規模での環境の悪化により,これらのニーズに加え環境に配慮した生産技術の確立と普及が急務となっている。
育苗箱全量施肥(以後,箱施肥)は,施肥窒素の利用率が極めて高いことから環境保全型栽培技術として注目されている。ところが,慣行栽培に比べ玄米の品質・食味・収量は同等の評価が多く,高品質・良食味米の安定生産技術とはなっていない。
今後,環境に配慮した生産技術が生産現場に持続的に普及・定着するためには,経営的に合理性を有することが重要であり,環境負荷が少ないことに加え収量・品質・食味の向上により農家収入が向上する技術であることが不可欠である。
秋田県では,2001年から分げつの発生次位・節位に着目した高品質・良食味米安定生産技術の確立に関する研究を実施し,その中で箱施肥と密植栽培を組み合わせた高品質・良食味米の安定生産技術を確立した。ここでは,その栽培理論と箱施肥による高品質・良食味米の安定生産技術を紹介する。
なお,試験は秋田県の主力良食味米品種である「あきたこまち」を供試品種とし,葉齢4.1~4.5葉(不完全葉を第1葉とする)の中苗移植栽培で試験を実施した。また,第N葉の基部から発生した1次分げつをTn,すべての2次分げつをTn’,主茎をMと表記した。そして,品質,食味の指標はそれぞれ整粒歩合,精玄米タンパク質含有率とし,収量は粒厚1.9mm以上の精玄米重で示した。

2)分げつの発生次位・節位理論による高品質・良食味米安定生産
水稲の収量は穂数と一穂精玄米重の積で決まる。穂数は分げつの発生頻度と穂への有効化率により決定される。したがって,安定生産のためには気象の変化にかかわらず分げつの発生頻度と穂への有効化率が安定して高く,一穂精玄米重が重い分げつを主体に穂数を確保することが重要である。
「あきたこまち」の中苗移植栽培では,MおよびT4~T7(以後,強勢茎)がそれ以外の分げつ(以後,弱勢茎)に比べて安定して分げつの発生頻度や穂への有効化率が高く1穂精玄米重が重い傾向にあった。また,栽植密度21.2株m-2で1株4本植えの慣行栽培を想定すると,強勢茎により確保できる穂数は424本m-2で目標収量を5.70t ha-1とした場合に必要な穂数はほぼ確保できる。さらに,強勢茎は弱勢茎に比べ着生粒の整粒歩合が高く,精米タンパク質含有率が低い傾向にあった。これらのことから,強勢茎は他の分げつに比べ高品質・良食味米安定生産に適していた1)。
また,弱勢茎を発生次第切除することによって有効茎歩合が高く強勢茎のみで構成される水稲群落を作成し,有効茎歩合の違いが収量,整粒歩合,精玄米タンパク質含有率に及ぼす影響について検討した。その結果,有効茎歩合の高い稲は低い稲に比べて,1穂精玄米重が重く,同時に整粒歩合が高く,精玄米タンパク質含有率が低い傾向にあった2)。
これらのことから,高品質・良食味米の安定生産において,強勢茎を主体に穂数を確保することに加えさらに有効茎歩合を高めることが重要であることを明らかにした。
3)箱施肥による高品質・良食味米安定生産技術
試験は,2002~2004年の3カ年に秋田県農業試験場内の水田圃場(細粒強グライ土)で実施した。試験区の構成と耕種条件は表1に示した。箱施肥区は,慣行区に比べ育苗期から分げつ発生始期にかけて肥料窒素の溶出が極めて少ないことからT4の発生頻度が低い(図2)。このため,栽植密度21.2株m-2,1株4本植えの栽培条件では,強勢茎のみで目標とする424本m-2の穂数を確保することができない。そこで,栽植密度を24.2株m-2の密植にした。

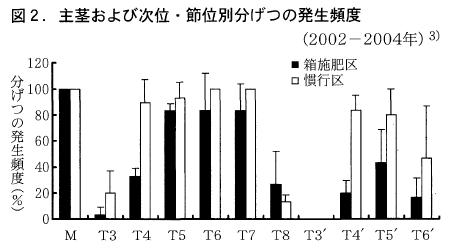
その結果,慣行区に比べ強勢茎主体に安定して目標穂数が確保され,穂への有効化率が低い2次分げつの発生数が少ないことから有効茎歩合が向上し(図3,図4),目標収量が安定して確保された(表2)。さらに,整粒歩合が向上し,玄米のタンパク質含有率が低下した(表2)。
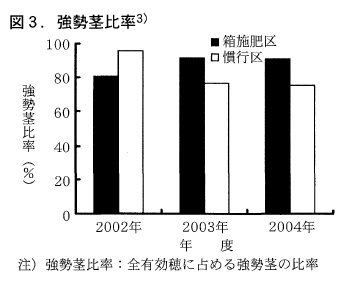
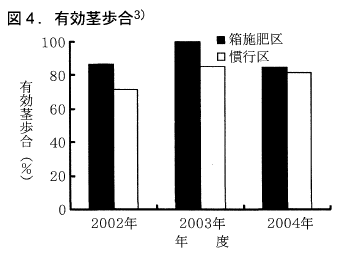
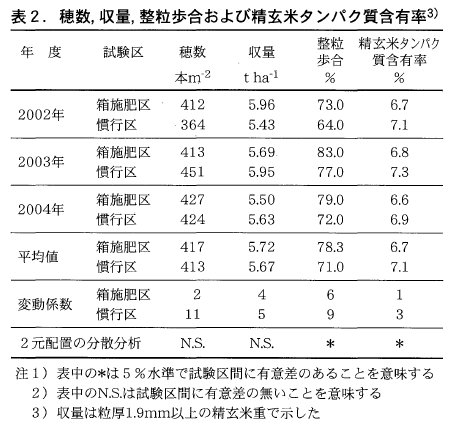
このように,箱施肥は密植にすることで強勢茎比率や有効茎歩合が向上し,安定した高品質・良食味米の生産が可能であった。
現在,箱施肥は減肥が可能であること,追肥が省略できることから省力技術として農家に普及している。そして,今後は密植を組み合わせることで環境保全型高品質・良食味米安定生産技術としてさらなる栽培面積の拡大が期待される。
文献
1)金和裕・金田吉弘・柴田智・佐藤馨・三浦恒子・佐藤敦:
中苗あきたこまちの高品質・良食味米安定生産に適した分げつの次位・節位,日作紀,74,149~155(2005)
2)三浦恒子・金和裕・佐藤馨・柴田智:
あきたこまちにおける有効茎歩合の向上が玄米の品質・食味に及ぼす影響:日作東北支部報,48,39~41(2005)
3)三浦恒子・金和裕・佐藤馨・柴田智:
育苗箱全量施肥栽培によるあきたこまちの高品質・良食味米安定生産,日作紀,74(別2),42~43(2005)

